У сучаснай медыцыне антыбіётыкі аказаліся адным з найбольш значных дасягненняў, значна знізіўшы ўзровень захворвання і смяротнасці, звязаныя з мікробнымі інфекцыямі. Іх здольнасць змяняць клінічныя вынікі бактэрыяльных інфекцый падоўжыла працягласць жыцця незлічоных пацыентаў. Антыбіётыкі маюць вырашальнае значэнне ў складаных медыцынскіх працэдурах, у тым ліку хірургічных умяшаннях, усталёўцы імплантаў, трансплантацыі і хіміятэрапіі. Аднак з'яўленне ўстойлівых да антыбіётыкаў патагенаў выклікае ўсё большую заклапочанасць, што з часам зніжае эфектыўнасць гэтых прэпаратаў. Выпадкі ўстойлівасці да антыбіётыкаў былі задакументаваны ва ўсіх катэгорыях антыбіётыкаў па меры ўзнікнення мікробных мутацый. Селекцыйны ціск, які аказваюць антымікробныя прэпараты, спрыяў узнікненню ўстойлівых штамаў, што стварае значную праблему для глабальнага здароўя.
Для барацьбы з актуальнай праблемай рэзістэнтнасці да антымікробных прэпаратаў неабходна ўкараняць эфектыўную палітыку кантролю інфекцый, якая абмяжоўвае распаўсюджванне ўстойлівых патагенаў, а таксама скарачае выкарыстанне антыбіётыкаў. Акрамя таго, існуе вострая патрэба ў альтэрнатыўных метадах лячэння. Гіпербарычная кіслародная тэрапія (ГБА) стала перспектыўным метадам у гэтым кантэксце, які ўключае ўдыханне 100% кіслароду пры пэўных узроўнях ціску на працягу пэўнага перыяду часу. Пазіцыянуемая як асноўны або дадатковы метад лячэння інфекцый, ГБА можа даць новую надзею ў лячэнні вострых інфекцый, выкліканых устойлівымі да антыбіётыкаў патагенамі.
Гэтая тэрапія ўсё часцей ужываецца ў якасці асноўнага або альтэрнатыўнага лячэння розных захворванняў, у тым ліку запалення, атручвання чадным газам, хранічных ран, ішэмічных захворванняў і інфекцый. Клінічнае прымяненне ГБА ў лячэнні інфекцый мае шырокія магчымасці і забяспечвае неацэнныя перавагі для пацыентаў.

Клінічнае прымяненне гіпербарычнай кіслароднай тэрапіі пры інфекцыях
Сучасныя дадзеныя пераканаўча пацвярджаюць карысць прымянення ГБА як самастойнага, так і дадатковага лячэння, што прыносіць значную карысць інфікаваным пацыентам. Падчас ГБА ціск кіслароду ў артэрыяльнай крыві можа павысіцца да 2000 мм рт.сл., а ў выніку высокі градыент ціску кіслароду ў тканінах можа павысіць узровень кіслароду ў тканінах да 500 мм рт.сл. Такія эфекты асабліва каштоўныя для садзейнічання гаенню запаленчых рэакцый і парушэнняў мікрацыркуляцыі, якія назіраюцца ў ішэмічных асяроддзях, а таксама для лячэння сіндрому кампартмента.
ГБАТ таксама можа ўплываць на станы, якія залежаць ад імуннай сістэмы. Даследаванні паказваюць, што ГБАТ можа падаўляць аўтаімунныя сіндромы і імунныя рэакцыі, выкліканыя антыгенам, дапамагаючы падтрымліваць талерантнасць да трансплантата, зніжаючы цыркуляцыю лімфацытаў і лейкацытаў, адначасова мадулюючы імунныя рэакцыі. Акрамя таго, ГБАТпадтрымлівае гаеннепры хранічных паражэннях скуры шляхам стымуляцыі ангіягенезу, крытычна важнага працэсу для паляпшэння аднаўлення. Гэтая тэрапія таксама спрыяе ўтварэнню калагенавай матрыцы, што з'яўляецца важнай фазай гаення ран.
Асаблівую ўвагу неабходна надаваць некаторым інфекцыям, асабліва глыбокім і цяжка лячым інфекцыям, такім як некратычны фасцыіт, астэаміэліт, хранічныя інфекцыі мяккіх тканін і інфекцыйны эндакардыт. Адным з найбольш распаўсюджаных клінічных ужыванняў ГБО з'яўляецца лячэнне інфекцый скуры і мяккіх тканін і астэаміэліту, звязаных з нізкім узроўнем кіслароду, якія часта выклікаюцца анаэробнымі або рэзістэнтнымі бактэрыямі.
1. Інфекцыі дыябетычнай ступні
Дыябетычная ступняЯзвы з'яўляюцца распаўсюджаным ускладненнем сярод пацыентаў з дыябетам, якое дзівіць да 25% гэтай папуляцыі. Інфекцыі часта ўзнікаюць у гэтых язвах (на іх долю прыпадае 40%-80% выпадкаў) і прыводзяць да павышэння захворвання і смяротнасці. Інфекцыі дыябетычнай ступні (ІДС) звычайна складаюцца з полімікробных інфекцый з рознымі анаэробнымі бактэрыяльнымі патагенамі. Розныя фактары, у тым ліку дэфекты функцыі фібрабластаў, праблемы з утварэннем калагена, клеткавыя імунныя механізмы і функцыя фагацытаў, могуць перашкаджаць гаенню ран у пацыентаў з дыябетам. У некалькіх даследаваннях парушэнне аксігенацыі скуры было выяўлена як моцны фактар рызыкі ампутацый, звязаных з ІДС.
Як адзін з сучасных варыянтаў лячэння DFIПаведамлялася, што ГБАТ значна паскарае гаенне язваў дыябетычнай ступні, што, у сваю чаргу, зніжае неабходнасць ампутацый і складаных хірургічных умяшанняў. Гэта не толькі мінімізуе неабходнасць у рэсурсаёмістых працэдурах, такіх як лоскутавыя аперацыі і перасадка скуры, але і прадугледжвае меншыя выдаткі і мінімальныя пабочныя эфекты ў параўнанні з хірургічнымі метадамі. Даследаванне Чэня і інш. паказала, што больш за 10 сеансаў ГБАТ прывялі да паляпшэння гаення ран на 78,3% у пацыентаў з дыябетам.
2. Некратычныя інфекцыі мяккіх тканін
Некратычныя інфекцыі мяккіх тканін (НМТ) часта бываюць полімікробнымі, звычайна ўзнікаюць з-за спалучэння аэробных і анаэробных бактэрыяльных патагенаў і часта асацыююцца з газаўтварэннем. Хоць НМТ сустракаюцца адносна рэдка, яны маюць высокі ўзровень смяротнасці з-за хуткага прагрэсавання. Своечасовая і правільная дыягностыка і лячэнне з'яўляюцца ключом да дасягнення спрыяльных вынікаў, і ГБАТ рэкамендуецца ў якасці дадатковага метаду лячэння НМТ. Нягледзячы на тое, што да гэтага часу існуюць спрэчкі адносна выкарыстання ГБАТ пры НМТ з-за адсутнасці праспектыўных кантраляваных даследаванняў,дадзеныя сведчаць аб тым, што гэта можа быць звязана з паляпшэннем выжывальнасці і захаваннем органаў у пацыентаў з неінвазіўнымі стыхійнымі захворваннямі (НСТІ)Рэтраспектыўнае даследаванне паказала значнае зніжэнне смяротнасці сярод пацыентаў з неінфекцыйнымі стыхіямі ствалавых тканак (НСТІ), якія атрымліваюць ГБАТ.
1.3 Інфекцыі хірургічнага ўмяшання
Інфекцыйныя ірвоты і ірвоты могуць быць класіфікаваны ў залежнасці ад анатамічнага месца інфекцыі і могуць узнікаць з-за розных патагенаў, у тым ліку як аэробных, так і анаэробных бактэрый. Нягледзячы на прагрэс у мерах кантролю інфекцый, такіх як метады стэрылізацыі, выкарыстанне прафілактычных антыбіётыкаў і ўдасканаленне хірургічнай практыкі, інфекцыі і ірвоты застаюцца пастаянным ускладненнем.
У адным значным аглядзе даследавалася эфектыўнасць ГБАТ ў прафілактыцы глыбокіх хірургічных траўмаў вобласці кішачніка (ХКМ) пры аперацыях на нервова-мышачным скаліёзе. Перадаперацыйная ГБАТ можа значна знізіць частату ХКМ і палегчыць гаенне ран. Гэтая неінвазіўная тэрапія стварае асяроддзе, у якім узровень кіслароду ў тканінах раны павышаны, што асацыюецца з акісляльным знішчальным дзеяннем на патагены. Акрамя таго, яна ліквідуе паніжаны ўзровень кіслароду ў крыві і кіслароду, якія спрыяюць развіццю ХКМ. Акрамя іншых стратэгій кантролю інфекцый, ГБАТ рэкамендуецца асабліва для аперацый з чыстай забруджанай паверхняй, такіх як каларэктальныя працэдуры.
1.4 Апёкі
Апёкі — гэта траўмы, выкліканыя моцнай спякотай, электрычным токам, хімічнымі рэчывамі або радыяцыяй, і яны могуць прывесці да высокага ўзроўню захворвання і смяротнасці. ГБАТ карысная пры лячэнні апёкаў, павялічваючы ўзровень кіслароду ў пашкоджаных тканінах. Хоць даследаванні на жывёлах і клінічныя даследаванні паказваюць неадназначныя вынікі адноснаэфектыўнасць ГБО пры лячэнні апёкаўДаследаванне з удзелам 125 пацыентаў з апёкамі паказала, што ГБАТ не аказала істотнага ўплыву на смяротнасць або колькасць выкананых аперацый, але скараціла сярэдні час гаення (19,7 дня ў параўнанні з 43,8 днямі). Інтэграцыя ГБАТ з комплексным лячэннем апёкаў можа эфектыўна кантраляваць сепсіс у пацыентаў з апёкамі, што прывядзе да скарачэння часу гаення і зніжэння патрэбы ў вадкасці. Аднак, каб пацвердзіць ролю ГБАТ у лячэнні шырокіх апёкаў, неабходныя далейшыя шырокія праспектыўныя даследаванні.
1.5 Астэаміэліт
Астэаміэліт — гэта інфекцыя костак або касцявога мозгу, часта выкліканая бактэрыяльнымі патагенамі. Лячэнне астэаміэліту можа быць складаным з-за адносна дрэннага кровазабеспячэння костак і абмежаванага пранікнення антыбіётыкаў у касцявы мозг. Хранічны астэаміэліт характарызуецца персістуючай інфекцыяй костак, лёгкім запаленнем і некратычным утварэннем касцяной тканіны. Рэфрактарны астэаміэліт — гэта хранічныя інфекцыі костак, якія працягваюцца або рэцыдывуюць, нягледзячы на адпаведнае лячэнне.
Было паказана, што ГБАТ значна паляпшае ўзровень кіслароду ў інфікаваных касцяных тканінах. Шматлікія серыі выпадкаў і кагортныя даследаванні паказваюць, што ГБАТ паляпшае клінічныя вынікі для пацыентаў з астэаміэлітам. Здаецца, што яна дзейнічае праз розныя механізмы, у тым ліку павышае метабалічную актыўнасць, падаўляе бактэрыяльныя патагены, узмацняе эфекты антыбіётыкаў, мінімізуе запаленне і спрыяе гаенню.працэсы. Пасля ГБО ў 60–85 % пацыентаў з хранічным, рэфрактарным астэаміэлітам назіраюцца прыкметы падаўлення інфекцыі.
1.6 Грыбковыя інфекцыі
Ва ўсім свеце больш за тры мільёны чалавек пакутуюць ад хранічных або інвазіўных грыбковых інфекцый, што штогод прыводзіць да больш чым 600 000 смерцяў. Вынікі лячэння грыбковых інфекцый часта пагаршаюцца з-за такіх фактараў, як змяненне імуннага статусу, асноўныя захворванні і характарыстыкі вірулентнасці патагенаў. ГБАТ становіцца прывабным тэрапеўтычным варыянтам пры цяжкіх грыбковых інфекцыях дзякуючы сваёй бяспецы і неінвазіўнай прыродзе. Даследаванні паказваюць, што ГБАТ можа быць эфектыўнай супраць грыбковых патагенаў, такіх як Aspergillus і Mycobacterium tuberculosis.
ГБАТ спрыяе супрацьгрыбковаму ўздзеянню, інгібіруючы ўтварэнне біяплёнкі Aspergillus, прычым павышаная эфектыўнасць назіраецца ў штамаў, у якіх адсутнічаюць гены супероксіддысмутазы (СОД). Гіпаксічныя ўмовы падчас грыбковых інфекцый ствараюць праблемы з дастаўкай супрацьгрыбковых прэпаратаў, што робіць павышэнне ўзроўню кіслароду з дапамогай ГБАТ патэнцыйна карысным умяшаннем, хоць неабходныя далейшыя даследаванні.
Антымікробныя ўласцівасці ГБО
Гіпераксічнае асяроддзе, якое ствараецца ГБА, ініцыюе фізіялагічныя і біяхімічныя змены, якія стымулююць антыбактэрыйныя ўласцівасці, што робіць яго эфектыўнай дадатковай тэрапіяй інфекцыі. ГБА дэманструе выдатныя эфекты супраць аэробных і пераважна анаэробных бактэрый праз такія механізмы, як прамая бактэрыцыдная актыўнасць, узмацненне імунных рэакцый і сінергічны эфект са спецыфічнымі антымікробнымі прэпаратамі.
2.1 Прамыя антыбактэрыйныя эфекты ГБАТ
Прамы антыбактэрыйны эфект ГБО ў значнай ступені абумоўлены ўтварэннем актыўных формаў кіслароду (АФК), якія ўключаюць супероксидныя аніёны, перакіс вадароду, гідраксільныя радыкалы і гідраксільныя іёны, якія ўзнікаюць падчас клеткавага метабалізму.
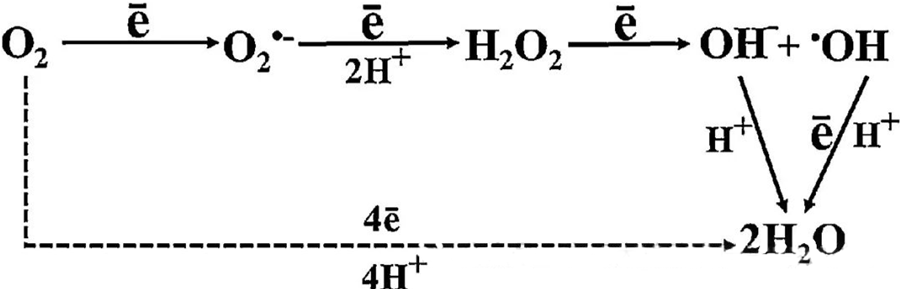
Узаемадзеянне паміж O₂ і клеткавымі кампанентамі мае важнае значэнне для разумення таго, як утвараюцца актыўныя кіслароды (АФК) у клетках. Пры пэўных умовах, якія называюцца акісляльным стрэсам, баланс паміж утварэннем АФК і іх дэградацыяй парушаецца, што прыводзіць да павышэння ўзроўню АФК у клетках. Выпрацоўка супераксіду (O₂⁻) каталізуецца супераксіддысмутазай, якая пасля пераўтварае O₂⁻ у пераксід вадароду (H₂O₂). Гэта пераўтварэнне яшчэ больш узмацняецца рэакцыяй Фентана, якая акісляе Fe²⁺ з утварэннем гідраксільных радыкалаў (·OH) і Fe³⁺, тым самым ініцыюючы шкодную акісляльна-аднаўленчую паслядоўнасць утварэння АФК і пашкоджання клетак.
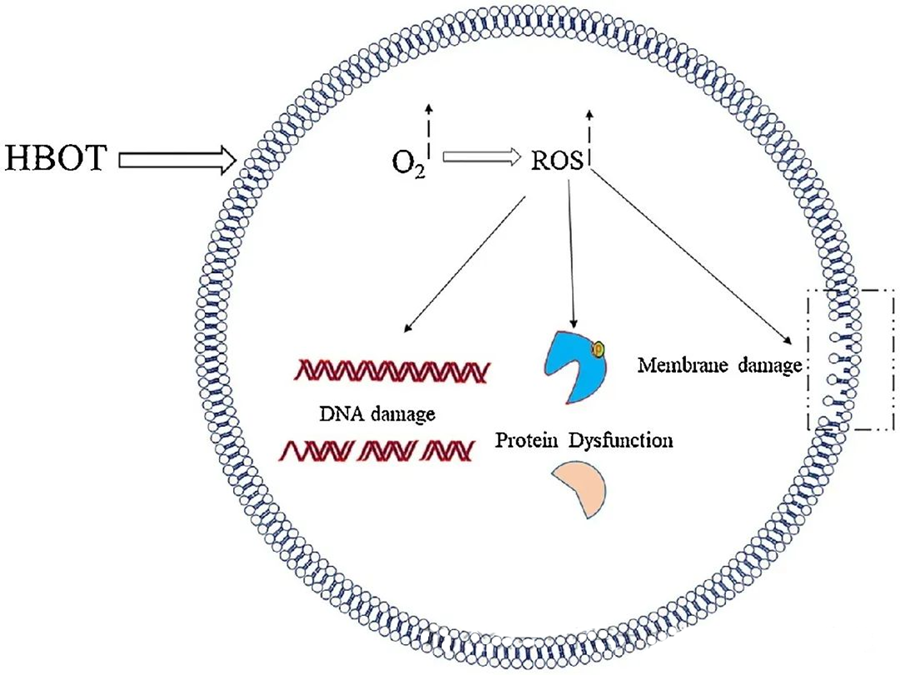
Таксічны эфект АРК накіраваны на крытычна важныя клеткавыя кампаненты, такія як ДНК, РНК, бялкі і ліпіды. Прыкметна, што ДНК з'яўляецца асноўнай мішэнню цытатаксічнасці, апасродкаванай H₂O₂, паколькі яна парушае структуры дэзоксірыбозы і пашкоджвае асноўныя кампаненты. Фізічнае пашкоджанне, выкліканае АРК, распаўсюджваецца на спіральную структуру ДНК, што можа быць вынікам перакіснага акіслення ліпідаў, выкліканага АРК. Гэта падкрэслівае неспрыяльныя наступствы падвышанага ўзроўню АРК у біялагічных сістэмах.
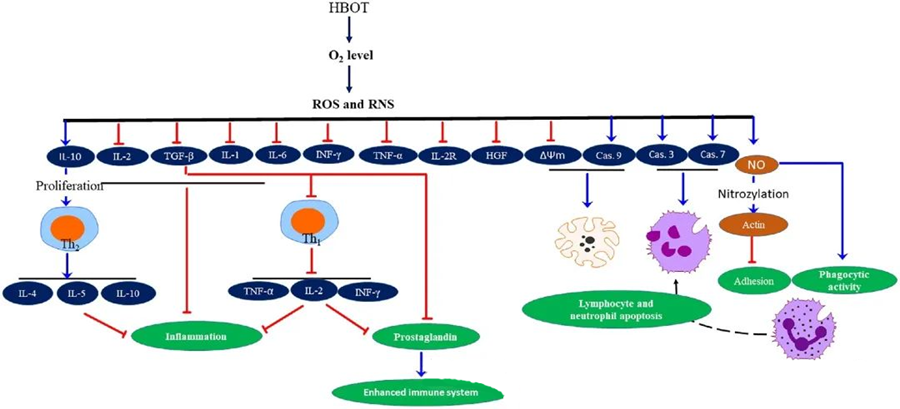
Антымікробнае дзеянне АРК
АФК адыгрываюць жыццёва важную ролю ў падаўленні росту мікробаў, што паказана на прыкладзе генерацыі АФК, выкліканай ГБАТ. Таксічны эфект АФК непасрэдна накіраваны на клетачныя кампаненты, такія як ДНК, бялкі і ліпіды. Высокія канцэнтрацыі актыўных формаў кіслароду могуць непасрэдна пашкоджваць ліпіды, што прыводзіць да перакіснага акіслення ліпідаў. Гэты працэс парушае цэласнасць клеткавых мембран і, адпаведна, функцыянальнасць мембраназвязаных рэцэптараў і бялкоў.
Акрамя таго, бялкі, якія таксама з'яўляюцца значнымі малекулярнымі мішэнямі АРК, падвяргаюцца спецыфічным акісляльным мадыфікацыям у розных амінакіслотных рэштках, такіх як цыстэін, метыянін, тыразін, фенілаланін і трыптафан. Напрыклад, было паказана, што ГБОТ выклікае акісляльныя змены ў некалькіх бялках E. coli, у тым ліку ў фактары элангацыі G і DnaK, тым самым уплываючы на іх клетачныя функцыі.
Павышэнне імунітэту з дапамогай ГБАТ
Супрацьзапаленчыя ўласцівасці ГБОТбылі дакументальна пацверджаны, што мае вырашальнае значэнне для палягчэння пашкоджання тканін і падаўлення прагрэсавання інфекцыі. ГБАТ істотна ўплывае на экспрэсію цытакінаў і іншых рэгулятараў запалення, уплываючы на імунную рэакцыю. Розныя эксперыментальныя сістэмы назіралі розныя змены ў экспрэсіі генаў і генерацыі бялку пасля ГБАТ, якія альбо павялічваюць, альбо паніжаюць фактары росту і цытакіны.
Падчас працэсу ГБАТ павышаны ўзровень O₂ выклікае шэраг клеткавых рэакцый, такіх як падаўленне вызвалення прозапаленчых медыятараў і стымуляванне апаптозу лімфацытаў і нейтрофілаў. У сукупнасці гэтыя дзеянні ўзмацняюць антымікробныя механізмы імуннай сістэмы, тым самым спрыяючы гаенню інфекцый.
Акрамя таго, даследаванні паказваюць, што павышэнне ўзроўню O₂ падчас ГБО можа знізіць экспрэсію прозапаленчых цытакінаў, у тым ліку інтэрферону-гама (IFN-γ), інтэрлейкіну-1 (IL-1) і інтэрлейкіну-6 (IL-6). Гэтыя змены таксама ўключаюць зніжэнне суадносін CD4:CD8 Т-клетак і мадуляцыю іншых растваральных рэцэптараў, што ў канчатковым выніку павышае ўзровень інтэрлейкіну-10 (IL-10), які мае вырашальнае значэнне для супрацьдзеяння запаленню і садзейнічання гаенню.
Антымікробная актыўнасць ГБО пераплецена са складанымі біялагічнымі механізмамі. Паведамлялася, што як супераксід, так і падвышаны ціск непаслядоўна спрыяюць антыбактэрыйнай актыўнасці, выкліканай ГБО, і апаптозу нейтрофілаў. Пасля ГБО значнае павышэнне ўзроўню кіслароду ўзмацняе бактэрыцыдныя здольнасці нейтрофілаў, што з'яўляецца важным кампанентам імуннай рэакцыі. Акрамя таго, ГБО падаўляе адгезію нейтрофілаў, якая апасродкавана ўзаемадзеяннем β-інтэгрынаў на нейтрофілах з малекуламі міжклеткавай адгезіі (ICAM) на эндатэліяльных клетках. ГБО інгібіруе актыўнасць нейтрофільнага β-2 інтэгрыну (Mac-1, CD11b/CD18) праз працэс, апасродкаваны аксідам азоту (NO), спрыяючы міграцыі нейтрофілаў да месца інфекцыі.
Дакладная перабудова цыташкілета неабходная для таго, каб нейтрофілы эфектыўна фагацытавалі патагены. Было паказана, што S-нітразіляванне актыну стымулюе палімерызацыю актыну, што патэнцыйна спрыяе фагацытарнай актыўнасці нейтрофілаў пасля папярэдняй апрацоўкі ГБО. Больш за тое, ГБО спрыяе апоптозу ў Т-клеткавых лініях чалавека праз мітахандрыяльныя шляхі, прычым паведамлялася пра паскораную гібель лімфацытаў пасля ГБО. Блакаванне каспазы-9 без уздзеяння на каспазу-8 прадэманстравала імунамадулюючыя эфекты ГБО.
Сінергічны эфект ГБАТ з антымікробнымі прэпаратамі
У клінічнай практыцы ГБАТ часта выкарыстоўваецца разам з антыбіётыкамі для эфектыўнай барацьбы з інфекцыямі. Гіпероксічны стан, які дасягаецца падчас ГБАТ, можа паўплываць на эфектыўнасць некаторых антыбіётыкаў. Даследаванні паказваюць, што пэўныя бактэрыцыдныя прэпараты, такія як β-лактамы, фторхіналоны і амінагліказіды, дзейнічаюць не толькі праз уласцівыя механізмы, але і часткова абапіраюцца на аэробны метабалізм бактэрый. Такім чынам, прысутнасць кіслароду і метабалічныя характарыстыкі патагенаў маюць вырашальнае значэнне пры ацэнцы тэрапеўтычнага эфекту антыбіётыкаў.
Існуюць значныя доказы таго, што нізкі ўзровень кіслароду можа павысіць рэзістэнтнасць Pseudomonas aeruginosa да піперацыліну/тазабактаму, і што асяроддзе з нізкім утрыманнем кіслароду таксама спрыяе павышэнню рэзістэнтнасці Enterobacter cloacae да азітраміцыну. І наадварот, некаторыя гіпаксічныя ўмовы могуць павысіць адчувальнасць бактэрый да антыбіётыкаў тэтрацыклінавага шэрагу. ГБАТ служыць жыццяздольным дадатковым тэрапеўтычным метадам, стымулюючы аэробны метабалізм і рэаксігенуючы гіпаксічна інфікаваныя тканіны, што пасля павялічвае адчувальнасць патагенаў да антыбіётыкаў.
У даклінічных даследаваннях камбінацыя ГБАТ (якая ўводзілася двойчы на дзень на працягу 8 гадзін пад ціскам 280 кПа) разам з табраміцынам (20 мг/кг/сут) значна знізіла бактэрыяльную нагрузку пры інфекцыйным эндакардыце, выкліканым залацістым стафілакокам. Гэта дэманструе патэнцыял ГБАТ як дапаможнага лячэння. Далейшыя даследаванні паказалі, што пры тэмпературы 37°C і ціску 3 ATA на працягу 5 гадзін ГБАТ значна ўзмацняла эфекты іміпенему супраць Pseudomonas aeruginosa, інфікаванай макрафагамі. Акрамя таго, было ўстаноўлена, што камбінаваны метад ГБАТ з цэфазалінам аказаўся больш эфектыўным пры лячэнні астэаміэліту, выкліканага залацістым стафілакокам, на жывёльных мадэлях у параўнанні з цэфазалінам асобна.
ГБАТ таксама значна павялічвае бактэрыцыднае дзеянне цыпрафлаксацыну супраць біяплёнак Pseudomonas aeruginosa, асабліва пасля 90 хвілін уздзеяння. Гэта ўзмацненне тлумачыцца ўтварэннем эндагенных актыўных формаў кіслароду (АФК) і праяўляе павышаную адчувальнасць у мутантаў з дэфектам пераксідазы.
У мадэлях плеўрыту, выкліканага метыцылін-рэзістэнтным залацістым стафілакокам (MRSA), сумесны эфект ванкаміцыну, тэйкапланіну і лінезаліду з ГБАТ паказаў значна павышаную эфектыўнасць супраць MRSA. Метранідазол, антыбіётык, які шырока выкарыстоўваецца для лячэння цяжкіх анаэробных і полімікробных інфекцый, такіх як інфекцыі дыябетычнай ступні (ІДС) і інфекцыі месца хірургічнага ўмяшання (ІХУ), прадэманстраваў больш высокую антымікробную эфектыўнасць у анаэробных умовах. Неабходныя будучыя даследаванні для вывучэння сінергічнага антыбактэрыйнага эфекту ГБАТ у спалучэнні з метранідазолам як in vivo, так і in vitro.
Антымікробная эфектыўнасць ГБО ў дачыненні да рэзістэнтных бактэрый
З эвалюцыяй і распаўсюджваннем рэзістэнтных штамаў традыцыйныя антыбіётыкі з цягам часу часта губляюць сваю эфектыўнасць. Акрамя таго, ГБАТ можа аказацца неабходнай у лячэнні і прафілактыцы інфекцый, выкліканых патагенамі з множнай лекавай устойлівасцю, выступаючы ў якасці крытычнай стратэгіі, калі лячэнне антыбіётыкамі не атрымліваецца. Шматлікія даследаванні паведамлялі пра значны бактэрыцыдны эфект ГБАТ на клінічна значныя рэзістэнтныя бактэрыі. Напрыклад, 90-хвілінны сеанс ГБАТ пры ціску 2 атм істотна знізіў рост MRSA. Акрамя таго, у мадэлях суадносін ГБАТ павялічыў антыбактэрыйны эфект розных антыбіётыкаў супраць інфекцый MRSA. Паведамленні пацвердзілі, што ГБАТ эфектыўная ў лячэнні астэаміэліту, выкліканага Klebsiella pneumoniae, якая прадукуе OXA-48, без неабходнасці выкарыстання якіх-небудзь дадатковых антыбіётыкаў.
Карацей кажучы, гіпербарычная кіслародная тэрапія ўяўляе сабой шматгранны падыход да кантролю інфекцый, узмацняючы імунную рэакцыю, а таксама павялічваючы эфектыўнасць існуючых антымікробных прэпаратаў. Дзякуючы ўсебаковым даследаванням і распрацоўкам, яна мае патэнцыял для змякчэння наступстваў антыбіётыкарэзістэнтнасці, што дае надзею ў бягучай барацьбе з бактэрыяльнымі інфекцыямі.
Час публікацыі: 28 лютага 2025 г.

